
|
هموستاز :
هموستاز عبارت است از فرايند پيشگيري از دفع خون از عروق سالم و توقف خونريزي از عروق آسيب ديده . پيشگيري از دفع خون از عروق سالم نياز به تعداد كافي از پلاكت هاي كارآمد دارد زيرا پلاكت ها ،آندوتليوم را حمايت كرده و سبب حفظ ديواره عروق مي شوند. در توقف خونريزي ، فرايند هموستاز دخالت دارد.
پاتوفيزيولوژي:
بدن انسان توسط مكانيسم هاي پيچيده و وابسته به هم در مقابل خونريزي هاي شديد و كشنده حفاظت مي شود. هموستاز شامل4 مرحله است:
مرحله ي اول يا مرحله ي عروقي : به شكل انقباض فوري رگ هاي صدمه ديده انجام مي شود. اسپاسم ايجاد شده در اين رگ ها براي متوقف كردن خونريزي مويرگي كافي است.
بلافاصله به دنبال بریدگی یا پارگی رگ ، صدمه ی وارد شده به دیواره ی آن موجب انقباض رگ می شود . این امر بی درنگ موجب کاهش جریان خون از محل بریدگی می شود .
انقباض مذکور از 3 عامل ناشی می شود :
1 – اسپاسم عضلانی موضعی
٢ – عوامل اتاکوئید موضعی که از بافتها و پلاکتهای خونی آسیب دیده رها می شوند
٣- رفلکس های عصبی
رفلکس های عصبی به واسطه ی پیام های عصبی درد و یا سایر
کربوهیدرات به پلی هیدروکسی آلدئید یا پلی هیدروکسی کتون و یا ترکیباتی که به این دو گروه هیدرولیز میشوند اطلاق میگردد.دسته ای از کربوهیدراتها را که نمیتوانند به ترکیب ساده تری شکسته شوند. مونوساکارید میگویند. گروهی را که در اثر هیدرولیز به دو مولکول مونوساکارید تجزیه شوند دی ساکارید و بالاخره کربوهیدراتهایی که به چندین واحد مونو ساکارید تجزیه میشوند را اولیگوساکارید گویند و چنانچه تعداد واحدهای تشکیل دهندة آن بیش از شش عدد باشد پلی ساکارید نامیده میشود.
مونوساکاریدها را میتوان به دو گروه عمده تقسیم کرد: اگر مونوساکاریدها دارای عامل آلدئیدی باشند آنها را آلدوز و چنانچه عامل کتونی داشته باشند آنها را کتوز مینامند.
از لحاظ احیا کنندگی نیز قندها را به دو دسته احیا کننده و غیر احیا کننده تقسیم میکنند. قندهای احیا کننده به علت داشتن گروههای احیا کننده آلدئیدی یا کتونی دارای خاصیت فوق هستند. قندهای احیا کننده میتوانند یونهای فلزاتی مثل مس دو ظرفیتی (Cu2+) و یون نقره را در محیط قلیایی احیا کنند. مس دو ظرفیتی پس از احیا به صورت مس یک ظرفیتی (Cu+) در می آید. این یون کمتر از مس دو ظرفیتی در آب محلول است و در نتیجه به صورت رسوب سبز رنگ CuOH یا رسوب قرمز رنگ Cu2O و یا مخلوط زرد رنگی از این دو ترکیب در می آید. اگر PH محیط اسیدی شود (مانند آزمایش بارفورد) و همچنین زمان حرارت دادن کنترل شود، فقط مونو ساکاریدها به این آزمایش جواب مثبت میدهند.
آزمایش مولیش: اسید سولفوریک غلیظ باعث هیدرولیز اتصالات گلیکوزیدی شده، ایجاد مونوساکارید میکند. مونوساکارید تولید شده آب خود را از دست میدهد و به فورفورال و مشتقات آن تبدیل میشود. سپس این ترکیب با آلفا نفتل کمپلکس بنفش رنگی ایجاد میکند.
روش کار:
۵ میلی لیتر محلول قند را در یک لوله آزمایش ریخته، به آن دو قطره محلول آلفا نفتل اضافه کنید و خوب بهم بزنید. به دقت ۳ میلی لیتر اسید سولفوریک غلیظ از دیواره لوله اضافه کنید. اسید را به آرامی اضافه کنید تا محلول درون لوله به هم نخورد مشاهده می کنیم که مابین محلول قند و محلول آلفا نفتل کمپلکس بنفش رنگ ایجاد می شود .
منبع
يكي از مهمترين و پركاربردترين روشهاي جداسازي و تشخيص مواد مختلف از يكديگر در آزمايشگاه، كروماتوگرافي است. در مواقعي كه جداسازي به روشهاي ديگر ناممكن است به راحتي ميتوان از اين روش استفاده كرد...
لينك دانلود فايل كامل:

یا

منبع
آزمایش قانون بقای جرم دانلود
آزمایش تعیین سختی آب دانلود
آزمایش تیتراسیون اکسیداسیون-احیادانلود
آزمایش تیتراسیون اسید و باز دانلود
حجم : 1.08MB
فرمت : PDF
تعداد صفحات : 148
رمز فایل: www.bbook.ir
دانلود آز بیوشیمی 1

دانلود آز بیوشیمی 2

گزارش کار آزمایشگاه ژنتیک رشته زیست شناسی :
مشاهده و مطالعه مراحل تقسیم میتوز
آشنایی با مگس سرکه
آمیزش مونوهیبریدیسم
آمیزش دی هیبریدیسم
صفات وابسته به جنس
مشاهده ی کروموزوم های پلی تن
مطالعه کروماتین جنسی در یاخته های انسانی
گروه های خونی در انسان
تشخیص حس چشایی با ماده PTC
کروماتوگرافی رنگدانه های چشم مگس سرکه
حجم : 2.73 MB

رمز : www.iran-stu.com
این جزوه ی ارزشمند که توسط استاد پیام بهزادی تهیه و تدوین شده شامل تمامی سر فصل های درس آزمایشگاه قرچ شناسی بعلاوه ی گزارش کارهای این درس است که در اختیار شما عزیزان قرار میگیرد.
شامل:
طرز تهیه محیط کشت
تلقیح قارچ به محیط کشت (کشت نقطه ای - کشت لوله ای - کشت لام)
مراحل جداسازی قارچ از روی میوه ها
بررسی آزمایشگاهی انواع قارچ ها
جداسازی قارچ های خاکزی
مطالعه مخمرها
مطالعه گلسنگ ها
مطالعه ی میکروسکوپی قارچ های ماکروسکوپی
مطالعه قارچ های نماتدخوار
و ....
لینک دانلود
رمز فایل: www.bbooks.ir
مقدمه:
عناصر غذایی معدنی ، مرتبا بین موجودات زنده و محیط زندگیشان در گردش هستند. جذب مواد معدنی بوسیله گیاهان مرحلهای کلیدی در چرخش مواد معدنی در داخل بیوسفر است. گیاهان معدنچیان زمین بوده و از این طریق مواد غیر آلی ضروری برای رشد و تکثیر سایر موجودات را فراهم میسازند. ورود عناصر غذایی معدنی به بیوسفر ، از طریق سیستم ریشه گیاهان صورت میگیرد. بنابراین گسترش زیاد سطح ریشه و نیز توانایی ریشه در جذب غلظتهای مختلف مواد غذایی معدنی خاک در فرایند جذب عناصر بسیار موثر هستند. عناصر موجود در محیط غذایی خاک پس از یونیزاسیون جذب گیاهان شده و اشکال فلزی آنها به همان صورت مورد استفاده گیاهان قرار نمیگیرند. مثلا اگر احتیاجات گیاهان را نسبت به پتاسیم مورد توجه قرار دهیم این احتیاجات بوسیله کاتیونهای پتاسیم تامین میشود که از تفکیک یونی KCl بوجود میآید. یونها جذب ذرات کلوئیدی موجود در محیط خاک شده به صورت رونشینی در سطح خارجی آنها قرار می گیرند. در این صورت مبادله یون بین ذرات کلوئیدی مختلف انجام پذیر بوده و این یونها میتوانند تدریجا از ذرات کلوئیدی جدا شده و وارد ساختمان گیاه شوند
به طور کلی گياهان به 13عنصرمعدنى براى رشد نياز دارند تا چرخه زندگىشان را كامل كنند، این عناصر مواد غذايى ضرورى گياه ناميده مي شوند.هر كدام ازاين عناصريك نقش حياتى درگياهان دارند و هر بافت گياهى به مقدار متفاوتى از آنها نيازدارند. S، Mg ، Ca، K، P وN جزء عناصر پر مصرف گياهى هستند كه مقاديرزيادى از آنها در گياه لازم است. عناصر کم مصرف ( Fe، Cu، Mn ،Zn، Br، Mo، Cl) عناصرى هستند كه نسبت به عناصر عناصر پر مصرف گياه به مقداركمترى از آنها نياز دارد.علاوه بر اين عناصرغذايى معدنى وجود دارند که براى گياهان سودمند هستند اما الزامأ ضرورى نيستند مانند: Na، Ni ،Co ،Se ،Al ، Van . شکل عناصرغذايى كه توسط گياهان جذب مي شوند ازطريق تغيير عملكرد و نيزتحركشان در درگياه تغيير مي كنند.
برخى مواد غذايى مانند N، P، K، Mg ،Cl و...مي توانند به آسانى در گياه از قسمتهاى پير گياه به قسمتهاى فعال از نظررشد مانند برگهاى جوان حركت كنند. موادغذايى ديگر مانند S ،Ca، Fe، Bبه آسانى در گياه حركت نمي كنند
مقدمه:
شير هنگامي كه از غدد شیری دام سالم دوشيده شود، عاری از باکتری یا داراي تعداد بسيار كمي باكتري است. مقدار بار میکروبی کل یا شمارش کلی میکروبی در شیر ضمن اینکه به عنوان یک روش متداول و شاخص ترین معیار در روند ارزیابی کیفیت شیرخام است، به عنوان یکی از ملاکهای مهم پیش بینی سلامت گاو و بهداشت وضعیت شیردوشی و نشانگر چگونگی حمل و نقل و نگهداری شیرخام می باشد.
انتقال آلودگى باکتریایى از محیط شیردوشى و تجهیزات آن به شیر غیرقابل اجتناب است چرا که ههم فلور طبیعی سینه دام و هم فلور محیط خارج خیلی راحت به شیر انتقال پیدا می کنند، ولى با این حال شمارش کلى باکتریایى شیرى که تا حد مناسبى سرد شده و تحت شرایط مطلوبى تولید شده باشد، باید در حد کمتر از 10000 باکترى در هر میلى لیتر باقى بماند. اگر شمارش باکتریایى شیر به طور قابل ملاحظه اى افزایش یابد مثلاً به بیش از 3 میلیون در میلى لیتر برسد، چربى، پروتئین یا لاکتوز شیر تجزیه مى شود که این امر سبب به وجود آمدن بو و طعم نامطبوع در شیر شده و به طور چشمگیرى قابلیت نگهدارى و کاربرد شیر را کاهش مى دهد. تعداد کل باکتری های شیر در رابطه با ارزیابی مناسب آن برای مصرف انسان نه تنها مهم است، بلکه اهمیت بیشتر آن در امکان وجود باکتری هایی است که قادرند موجب ایجاد بیماری در مصرف کننده شوند. در این میان باکتری های بیماریزا چون بروسلا، استافیلوکوکوس ها، لیستریا، سل گاوی، کلی فرمها، سالمونلا و ..... که موجب بیماریهایی مثل تب مالت، سل، حصبه، لیستریوز، اسهال خونی و التهابات گوارشی می گردند، مهم هستند. كلي فرم ها، باسیل های گرم منفی، بدون اسپور، میله ای شکل، هوازی و یا بی هوازی اختیاری هستند كه می توانند در حرارت 30 الی 37 درجه سانتی گراد رشد كنند. اين موجودات بسادگي مي توانند باعث تخريب شير شده و در مدت 24 الی 48 ساعت لاكتوز را تخمیر کرده و به اسيد لاكتيك و گاز تبديل نمايند و پروتئين هاي موجود در شير را هم بشكنند. کلی فرم ها می توانند به عنوان درجه بندی میزان آلودگی فراورده های خام مورد بررسی قرار گیرند. منبع اصلی آنها روده حیوانات خون گرم است. نمونه بارز آن اشریشیا است، كه در اين دسته جاي مي گيرد. جنس اشریشیا شامل شش گونه است که گونه اشریشیاکلی گونه شاخص آن می باشد. اشریشیاکلی معمولترین میکروارگانیسم هوازی در دستگاه گوارش برخی حیوانات و انسان است و به عنوان معیار آلودگی آب و مواد غذایی به مدفوع مطرح می باشد.كلي فرم ها طي فرآيند پاستوريزاسيون و با حرارت سريع از بين مي روند و بعد از حرارت دادن، تكثير نمي يابند و حضورشان در شير بيانگر آلودگي ثانويه است. اشریشیاکلی از طریق آب، شیر و فراورده های آن و گوشت به انسان منتقل می شود. وجود کلی فرم های مدفوعی مانند اشریشیاکلی دلالت بر آلودگی شیرخام با مدفوع حیوانی و انسانی است. وجود آن در شیر پاستوریزه نشانه ناسالم بودن آن شیر برای مصرف انسانی است. بر اساس استاندارد های موجود لازم است تعداد کلی فرم در یک میلی لیتر شیرخام کمتر از 100 عدد باشد. هم چنین تعداد کلی فرم ها در یک میلی لیتر شیر پاستوریزه باید کمتر از 10 عدد و اشریشیا کلی در یک میلی لیتر شیر پاستوریزه نباید وجود داشته باشد.
از دیگر باکتری های موجود در شیر می توان استرپتوکوک ها، لاکتوباسیلوس ها، میکروکوکوس ها و ... را نام برد. تبQ ، عفونت های استرپتوکوکی، توبرکلوزیز، بروسلوزیز و ...نیز از مهمترین بیماری هایی هستند که توسط شیر ایجاد می شوند.
برای از بین بردن باکتری های شیر از پاستوریزه کردن استفاده می شود. پاستوريزه کردن را مىتوان چنين تعريف کرد؛ گرم کردن شير بهمدت و با درجهاى که براى نابود کردن هر گونه عامل بيمارىزائى احتمالى موجود در شير لازم است بهشرط آنکه کمترين دگرگونى را در ترکيب شير بهوجود آورد و طعم و ارزش غذائى آن را هم تغيير ندهد.
با پاستوريزه کردن، نزديک به نود درصد ميکروبهاى شير از بين مىروند؛ از جمله ميکروبهاى سل که بيشتر در گرما پايدار هستند و عامل تب Q ولى با پاستوريزه کردن نه هاگ ميکروبها و نه ميکروبهاى گرما پايدار از بين نمىروند و از اينرو با وجود پاستوريزه کردن شير، چون گرماى محيط بعداً بالا مىرود ميکروبها به فراوانى تکثير مىيابند و براى کنترل رشد خون زيستمندان شير پاستوريزه بهسرعت تا چهار درجه صد قسمتى خنک مىشود و بايد تا زمان مصرف خنک بماند. فرآوردههاى شير پاستوريزه در جاهاى گرمسير در گرماى هجده درجه صد قسمتى بيش از هشت تا دوازده ساعت بهداشتى و سالم نمىمانند.
یکی از آزمایش هایی که به منظور ارزیابی کیفیت باکتریایی شیر خام صورت می گیرد، آزمایش احیای متیلن بلو است. اساس این آزمایش احیای متیلن بلوی افزوده شده به شیر، در اثر فعالیت متابولیکی باکتری های آن و بی رنگ شدن متیلن بلو می باشد. این آزمایش مبتنی بر این است كه باكتری های موجود در شیر در دمای مناسب به سرعت رشد كرده و اكسیژن محیط را مصرف كنند در اثر مصرف اكسیژن ، حالت شیمیایی محیط تغییر كرده و پتانسیل اكسیداسیون و احیاء پایین می آید . برای تخمین زدن میزان فعالیت باكتری ها ، متیلن بلو ( شناساگر حالت اكسیداسیون و احیاء ) به شیر افزوده می شود . این شناساگر در ابتدا رنگ آبی دارد . اما پس از مصرف شدن اكسیژن محیط توسط باكتری های موجود در شیر رنگ خود را از دست داده و بی رنگ می شود .به طور كلی ، طول مدت احیاء با تعداد باكتری های موجود در شیر نسبت عكس دارد . یعنی هر چه تعداد باكتری ها زیاد تر باشد زمان كمتری برای تغییر رنگ متیلن بلو لازم است . برای تسریع رشد باكتری های موجود در شیر و كاهش طول مدت آزمایش ، پس از افزودن شناساگر ، باید نمونه شیر را در دمای كنترل شده قرار داد . اگر متیلن بلو در کمتر از 30 دقیقه بی رنگ شود، کیفیت شیر بسیار پایین بوده و در کلاس 4 قرار می گیرد. کلاس 3 شیرهایی هستند که کیفیت پایینی دارند و متیلن بلو در آنها پس از 30 دقیقه تا 2 ساعت بی نگ می شود.کلاس 2 کیفیت بهتری داشته و در مورد شیرهایی تعریف می شود که عمل احیای متیلن بلو در آنها بین 2 تا 6 ساعت انجام می شود.بهترین کیفیت شیر نیز زمانی است که متیلن بلو بتواند در آن تا 8 ساعت احیا نشده بماند. متیلن بلو دارای فرمول بسته C16H18N3SCl و فرمول ساختاری به شکل زیر است:
شرح آزمایش:
مواد و لوازم مورد نیاز: نمونه شیر ( در اینجا شیرهای استریل فروشی در سوپرمارکت ها) ، متیلن بلو ، محیط کشتNA ، پلیت، لوله آزمایش، آب مقطر استریل، بن ماری، انکوباتور، ورتکس و ...
روش کار:
الف) Reduction test : میز کار را کاملا استریل کرده و در کنار شعله روشن با استفاده از چاقوی استریل شده روی شعله در پاکت شیر را باز کرده و با استفاده از پیپت استریل، 10 میلی لیتر شیر را برداشته و به لوله آزمایش در دار استریل انتقال می دهیم. سر لوله آزمایش را با درپوش بسته و شیر را روی ورتکس 25 بار تکان می دهیم.سپس در کنار شعله یک میلی لیتر متیلن بلو به آن می افزایم ، در لوله را بسته و لوله را چند بار اینورت می کنیم تا رنگ کاملا با شیر مخلوط شود.سپس لوله را در بن ماری گذاشته و برای بار اول پس از 5 دقیقه بیرون آورده و 3 بار اینورت کرده و مجددا در بن ماری می گزاریم.برای دفعات بعد این کار را با فاصله های زمانی 30 دقیقه انجام می دهیم و هر بار تغییر رنگ را بررسی می کنیم تا ببینم متیلن بلو پس از چه زمانی بی رنگ می شود.
ب) تست Colony count : این تست برای شمارش میکرو ارگانیسم های موجود در شیر انجام می شود. از شیر سریال دایلوشن تهیه می کنیم.بدین طریق که یک سی سی از شیر را در کنار شعله به یک لوله آزمایش حاوی 9 میلی لیتر آب استریل در افزوده و پس از پنبه گذاری چند بار تکان داده و بعد با چند بار پیپتینگ محلول را یکنواخت کرده و یک سی سی از آن را برداشته و به لوله آزمایش دیگری که آن نیز حاوی 9 سی سی آب مقطر استریل است انتقال می دهیم. این کارها را تا جایی تکرار می کنیم که تمامی رقت های مورد آزمایش را داشته باشیم( رقت های 0.1، 0.01، 0.001 و ...). سپس از هر رقت یک سی سی برداشته و در کنار شعله درون پلیت استریل ریخته و کشت پور پلیت را برای آن انجام می دهیم.
پس از انکوباسیون گذاری و گذشت زمان، رشد کلنی های باکتریایی را در پلیت ها بررسی می کنیم. با شمارش کلنی ها و ضرب تعداد کلنی در عکس رقت میزان باکتری در یک سی سی از شیر مورد آزمایش به دست می آید
منبع:www.iran-stu.com/.
مقدمه:
نقطه شروع بسیاری از روشهای بیولوژی مولکولی و تشخیصی ، جدا سازی DNA با درجه خلوص بالا می باشد. دستورالعمل استخراج DNA با پشتوانه ای از دانش بیوشیمی همراه است و نباید صرفاً استفاده از چند ماده انگاشته شود . درک عملکرد هر ماده این امکان را فراهم خواهد نمود که در صورت نبود یک ماده ، از ماده دیگری با کار مشابه استفاده کرد . شیوه هایی که جهت خالص سازی DNA مورد استفاده قرار می گیرد علاوه بر برخورداری از حداقل زمان و سرعت بالا ، روش مطمئنی جهت حذف ممانعت کننده ها (inhibiators) و خالص نموده کلیه اسید های نوکلئیک نیز باشد . این ممانعت کننده ها گوناگون بوده و می توانند در ارتباط به نوع نمونه متفاوت باشند . در صورتیکه خالص نمودن DNA در نمونه از کیفیت پایینی برخوردار باشد ، بواسطه اثر مهار کنندگی مواد موجود در نمونه ها و یا مواد استفاده شده در مراحل خالص سازی ، بر فعالیت پلیمراز اثر گذاشته و نتیجه تست منفی کاذب خواهد گردید.
روشهای مختلفی برای استخراج DNA از میوه ها و پیاز ارائه شده اند که دلایل زیر برای اعمالی که در این روشهای مختلف انجام می شود ذکر می گردد:
1-چلیت کردن کاتیون های دو ظرفیتی مانند Ca2+, Mg2+ به وسیله نمکبرای متوقف کردن اعمال آنزیم تجزیه کنندهDNA (دی ان آزDNase-) همچنین نمک می تواند انتهاهای فسفات DNA را به هم نزدیک کند و در نتیجه رسوب آن را آسانتر نماید.
2-خرد کردن سلولها به وسیله رنده کردن
3- ازبین بردن لیپیدهای غشاء به وسیله اضافه کردن دترجنت و در نتیجه شکسته شدن غشاء
4-از بین بردن پروتئین های سلول و هیستون ها ی متصل به DNA به وسیله اضافه کردن یک پروتئاز و یا ته نشین کردن آنها با استات سدیم یا آمونیوم و یا نمک آشپزخانه
5-رسوب DNA در اتانول یا ایزوپروپانول سرد زیرا DNA در الکل نامحلول است اما در آب محلول است به هم می چسبند و این مرحله همچنین نمک را خارج می کند.
6-حرارت دادن(50 تا 60 درجه سانتی گراد) نه تنها به شکستن سلولها کمک می کند بلکه باعث غیر فعال شدن آنزیم های DNaseنیز می شود البته حرارت دادن اگر زیاد طول بکشد خود DNA را نیزتجزیه می کند. به همین علت در روشهائی که از حرارت استفاده می شود بایستی حد اکثر 12 دقیقه عصاره را در حمام آب گرم قرار داد و سپس بلافاصله جهت جلوگیری از انهدام DNA عصاره را در حمام آب سرد-یخ به مدت15 -5 دقیقه قرار داد.
7-کج نگاه داشتن لوله و سپس اضافه کردن الکل سرد مانع از مخلوط شدن عصاره و الکل میگردد و در نتیجه دو فاز تشکیل می گردد.
شرح آزمایش:
روی میز استریل شده در کنار شعله، یک لوپ ( تقریبا به اندازه یک عدس) باکتری از روی پلیت برمی داریم و در درون 200 میکرولیتر بافر TE درون یک ویال حل می کنیم. سپس مراحل زیر را به ترتیب برا آن انجام می دهیم( دقت شود که تمام مراحل در کنار شعله و کاملا استریل انجام شود و برای افزودن مواد از سمپلر مناسب استفاده شود.) :
- افزودن 20 میکرولیتر آنزیم لیزوزیم برای تخریب دیواره باکتریایی
- حرارت دهی در بن ماری در دمای 37 درجه به مدت 20 دقیقه
- افزودن 25 میکرولیتر SDS با غلظت 10 درصد جهت لیز سلولی ( برای تخلیص بیشتر دی ان ای می توان در صورت امکان از آنزیم پروتئاز به میزان 2.5 میکرولیتر و RNAase به میزان 3 میکرولیتر استفاده کرد.)
- افزودن 90 میکرولیتر SMNaCl به میزان 75 میکرولیتر
- انکوباسیون گذاری به مدت 10 دقیقه در فور با دمای 65 درجه سانتی گراد
- پروتئین زدایی با افزدون میزان هم حجم کلروفروم (تقریبا 200 میکرولیتر)
- سانتریفوژ ویال به مدت 5 دقیقه
- برداشتن مایع روی ویال و تکرار عمل پروتئین زدایی برای دو بار دیگر همراه با سانتریفوژ (می توان در این مرحله از فنل هم استفاده کرد.)
- رسوب دهی DNA با افزودن حدود0.6 حجم ماده، پروپانول (180میکرولیتر پروپانول) به ویال و سرمادهی آن به مدت 20 دقیقه در دمای 20- در فریزر
- سانتریفوژ با دور 8000 و به مدت 5 دقیقه
- شست و شو با الکل و سانتریفوژ مجدد
- دور ریختن محلول روی ویال ( کج کردن ویال و کشیده شدن آب با دستمال کاغذی؛ باید مراقب بود این کار با شدت انجام نشود چون موجب از دست رفتن رسوب دی ان ای می شود.) و صبر کردن تا خشک شدن کامل ویال
- افزودن 50 میکرولیتر از بافرTE به ویال
- تزریق محلول به ژل الکتروفورز و مشاهده نوارهای تشکیلی
نکته: برای نگه داری کوتاه مدت دی ان ای می توان از دمای 20- و برای نگه داری طولانی مدت آن باید از دمای 70- استفاده کرد.
منبع:www.iran-stu.com/
(البته مشاهداتش بسته به نوع خاکی که استفاده کردین متفاوته و من طبق ستون خودمون اونا رو نوشتم.هر چند محل دیدن انواع باکتریها همون چیزیه که ذکر شده.)
هدف: مشاهده ارتباط میکروارگانیسم ها با هم و بررسی چرخه عناصر و همینطور کشت باکتریهای مختلف در محیط شبیه سازی شده
مقدمه:
روش های مختلفی جهت شناسایی و مطالعه میکروارگانیسم های محیط وجود دارد. یکی از این روش های مهم و کارآمد ستون وینوگراوسکی است. ستون وینوگراوسکی اکوسیستم کوچک و کاملی است که جهت مطالعه اکولوژی میکروارگانیسم ها به کار گرفته می شود و به نام کاشف آن سرجی وینوگراوسکی معروف است. یکی از مهمترین کاربردهای این ستون این است که نشان می دهد چگونه میکروارگانیسم های مختلف یک اکوسیستم با هم ارتباط داشته و زمینه رشد و نمو همدیگر را مهیا یا مهار کنند. به عبارتی در نتیجه فعالیت یک میکروارگانیسم رشد دیگر میکروارگانیسم ها تحریک شده یا متوقف می شود.
میکروارگانیسم های مختلفی که در نمونه وجود دارند جهت رشد و نمو خود نیاز به شرایطی دارند که برای برخی از آنها شرایط مورد نیاز وجود داشته ولی برای برخی دیگر خصوصیات اولیه موجود شرایط مورد نیاز را مهیا نمی کنند. این شرایط مورد نیازشان در نتیجه رشد و نمو و نهایتاً فعالیت متابولیسمی گروهی از میکروارگانیسم ها که شرایط رشد آنها مهیا است، ایجاد می گردد. آنچه که در این ستون بایستی به آن توجه شود چگونگی ایجاد این شرایط یا وجود ارتباط بین میکروارگانیسم ها است.
در طبیعت بین میکروارگانیسم ها روابط مختلفی وجود دارد که به حالت های مختلفی یافت می شود. در ستون وینوگراوسکی می توان این روابط را مشاهده نمود جهت این امر نیاز است که شرایط خاصی در این ستون وجود داشته باشد که نیازمندی های رشد میکروارگانیسم ها را مهیا کند. نکته بسیار مهم و بسیار حائز اهمیت در این ستون، استفاده از آن جهت شناسایی یا ایزولاسیون باکتری خاصی از یک اکوسیستم است که در این مورد یکی از خصوصیات اصلی و بارز این میکروارگانیسم را در نظر گرفته و ستون وینوگراوسکی را براساس آن می سازیم. به عنوان مثال چنانچه هدف ایزولاسیون باکتری های دارای آنزیم پکتیناز باشد مواد دارای پکتین مانند کاه، ریشه درختان، برگ، گوشت، تخم مرغ و.... را به آن اضافه می کنیم و یا چنانچه هدف ایزولاسیون باکتری های دارای سلولز باشد به ستون به عنوان منبع کربن، تکه های کاغذ اضافه می شود.
شرح آزمایش:
استوانه ای بلند و شفاف را برای کار انتخاب کرده و ابتدا مقداری کاغذ را ریز کرده و به عنوان منبع کربن و یک قاشق سولفات کلسیم و کربنات کلسیم عنوان منبع کربن و گوگرد را با مقداری خاک مخلوط کرده و ته ستون می ریزیم. عمق این مواد باید حدودا 2 سانتی متر باشد. سپس روی آن خاک می ریزیم. این خاک باید مرطوب و نم دار و بدون سنگریزه باشد. بهتر است از گِل بدون سنگ استفاده کرد. سه چهارم ستون را با این خاک پر کرده و خاک را کاملا فشرده می کنیم تا بین آن هوا نماند و شرایط برای رشد باکتری های بی هوازی مهیا شود. سپس روی خاک، آب ریخته و ستون را در محلی که کاملا نورگیر باشد یا زیر چراغ مطالعه قرار می دهیم.
می توان پس از چندماه و رشد میکروارگانیسمها، از روی ستون نمونه گرفته و رنگ آمیزی کرد. برای این کار مقداری از خاک سبز رنگ دارای سیانوباکتر را برداشته و در آب حل می کنیم و پس از ته نشین شدن خاک با لوپ از روی آب نمونه گرفته و با کریستال ویوله رنگ آمیزی و مشاهده می کنیم. همچنین می توان یک قطره معلق را روی لام گذاشته و با گذاشتن لامل آن را مشاهده کرد.
مشاهدات :
در انتهای ستون رنگ سیاه مشاهده می شود که نشان دهنده رشد باکتری های بی هوازی اجباری در فضای به دور از نور و اکسیژن از سولفات و سلولز کاغذ استفاده می کنند. باکتری هایی مثل کلستریدیوم ها که از سلولز و دسولفوویبریوها که از سولفات به عنوان پذیرنده الکترون استفاده می کنند، در این ناحیه رشد می کنند.
کمی بالاتر از آن منطقه بی هوازی روشن است که باکتری های گوگردی های سبز و ارغوانی رشد کرده و ستون به رنگهای قرمز تیره و سبز در می آید.این باکتری ها از H2S آزاد شده توسط باکتری های دسولفوویبریو استفاده می کنند.
کمی بالاتر از باکتری های فوتوسنتز کننده گوگردی، باکتری های غیر گوگردی فوتوسنتز کننده رشد می کنند که ستون را به رنگ قرمز متمایل به بنفش در می آورند.
در بالاترین ناحیه ستون که غنی از اکسیژن است جلبک ها و سیانوباکترها با رنگ سبز به خوبی قابل رویت اند. با رنگ آمیزی خاک ناحیه رویی، باکتری های رشته مانند و طویل مشاهده می شوند که همان سیانوباکتری ها هستند. علاوه بر آن کوکسی های درشتی نیز مشاهده شدند.
در مشاهده لام قطره معلق نیز انواع و اقسام میکروارگانیسم های متحرک مشاهده شدند که شکل های متنوعی داشتند.از باکتری های کوکسی شکل و باسیل گرفته تا اشکال دوکی شکل با دیواره سبز رنگ. برخی از نمونه های مشاهده نیز دارای حرکت زنشی بودند.
خطاها:
- فشرده نشدن خاک به قدر کافی و به دام افتادن هوا در آن
- مناسب نبودن نمونه خاک
- نرسیدن نور به قدر کافی به ستون
منبع:www.iran-stu.com/
مشاهده کروموزوم های پلی تن

رمز : www.iran-stu.com
اجزای مختلف یاخته زنده به علت دارا بودن اختلاف غلظت و ضریب شکست بسیار کم به هنگام جذب طیف نور مرئی ، به قدر کافی کنتراست یا اختلاف میزان نور از خودشان نمیدهند. رنگهای زیستی ، بدون اینکه اندامکهای یاخته را بیجان سازند، آنها را بطور انتخابی رنگآمیزی میکنند. اساس و پایه رنگ آمیزی ترکیب مولکول های ماده رنگی مورد نظر با مولکول های اندام یا اجزای هدف می باشد. تعدادی از مواد رنگی به صورت رنگ عمومی کاربرد دارد و برخی ازرنگ ها مثل سبز ژانوس رنگ اختصاصی میتوکندری و یا قرمز خنثی برای رنگ آمیزی واکوئل است. رنگ های زیستی به رنگ هایی اطلاق می شود که هیچ گونه اثر سوئی در سلول های زنده نداشته باشند. با حفظ حیات نمونه اجزای مورد مطالعه به صورت اختصاصی رنگ می شوند. رنگ های حیاتی باید با غلظت پایین و شرایط اختصاصی از نظر PH و مولاریته تهیه شوند و مدت زمان رنگ آمیزی کوتاه باشد.
یک تعداد از رنگ های مورد استفاده رنگ های اسیدی و یک عده دیگر جز رنگ های بازی است که این مواد هم با قسمتهای آنیونی و کاتیونی غشای اندامک ها ترکیب می شوند و موجب رنگی شدن آن غشاها می شوند.
تشریح کرم خاکی
در طبقه بندی جانوران که در آغار قرن 19 قرن انجام گرفت، تمام جانورانی که دارای بدنی دراز و فاقد ضمایم واضح بودند به کرمها موسوم شدند. این جانوران به علت داشتن یک انتهای قدامی یا سر که دارای اندامهای حسی است و به قصد برخورد و روبرو شدن با محیط به طرف جلو حرکت میکنند و یک انتهای خلفی یا دم ، با اسفنجها و مرجانها و شانهداران اختلاف و تمایز دارند. رده کمتاران ، ردهای از کرمها هستند که به صورت حلقوی هستند که در هر حلقه چندین تار دارند. کرمهای خاکی نمونه ای از این رده است. از کرمهای خاکی بزرگ لومبریکوس ترستریس نمونه جالبی است که ممکن است به درازای 30 سانتیمتر و به قطر 9 میلیمتر رشد کند.
مشخصات خارجی
بدن این کرم ، استوانهای دراز و بطور واضح در دو انتها نازک و باریک است. سطح شکمی آن پهن و رنگ پریدهتر از سطح پشتی است و سطح پشتی تیره است. سر مشخص و متمایزی در حیوان وجود ندارد. بدن یک کرم بالغ به 80 تا 100 قطعه حلقهای شکل که بوسیله شیارهای عرض مجزا است، تقسیم شده است. دهان کرم در حلقه اول است و بوسیله یک قطعه گوشتی به نام پیش دهان آویزان میباشد. مخرج آن بیضی شکل و بطور عمودی در حلقه آخر قرار دارد. روی حلقههای 31 تا 37 برآمدگی غدهای واضحی به نام کمربند تناسلی دیده میشود. کمربند تناسلی ماده سازنده پیله را که محتوی تخم است ترشح میکند.
تارهای کرم خاکی
در هر حلقه به جز اولی و آخری ، 4 جفت تار موی مانند کوچک وجود دارد که در سطح شکمی و جانبی مختصر برجستگی پیدا کرده است. هر تار عبارت است از یک میله کیتینی نوک تیزی است که در یک کیسه اپیدرمی مخصوص واقع در درون دیواره بدن جای گرفته است. تار میتواند بوسیله عضلات منقبض کننده در هر جهت حرکت کرده، امتداد یابد و یا عقب کشیده شود و تارها در موقعی که کرم در سوراخش قرار دارد و یا روی زمین حرکت میکند مانند گیره یا میخ عمل مینماید.
دیواره بدن
قسمت خارجی کرم از یک کوتیکول شفاف و نازک پوشیده شده است.کوتیکول دارای خطوط عرضی نازکی است که یک منظره قوس و قزحی مختصری ایجاد میکند. در کوتیکول سوراخهایی در روی بسیاری از سلولهای حسی اپیدرم موجود است. اپیدرم روی یک غشای قاعدهای قراردارد و زیر غشای قاعدهای لایه نازکی از عضلات حلقوی و لایه ضخیمتری از عضلات طولی وجود دارد. سطح داخلی دیواره بدن از صفاق مستور است. شکل جانور در نتیجه خاصیت کشش دیواره بدن روی اندامها و مایعات درونی حفظ میشود.
دستگاه گوارش
این دستگاه از قسمتهای زیر تشکیل میشود:
- دهان که دنباله آن حفره دهانی است. (در حلقههای 3 – 1(
- حلق (در حلقههای 5 - 4) با غدههای مخصوص چرب و نرم کردن و الیاف عضلانی در دیوارههای خارجی آن.
- مری باریک و مستقیم (در حلقههای 14 - 6) که بوسیله سه جفت غدههای آهکی از پهلو اتصال دارد.
- یک چینهدان بزرگ با دیواره نازک که در حقیقت یک پیشخانه برای ذخیره میباشد.
- سنگدان (در حلقههای 18 - 17) با دیوارههای عضلانی ضخیم و محکم که در داخل از کوتیکول مفروش است.
- روده که تا مخرج امتداد دارد.
دستگاه گردش خون
خون در تمام قسمتهای بدن کرم جاری است و یک سیستم رگهای خونی بسته با مویرگها وجود دارد. پنج رگ اصلی ممتد در طول بدن و پنج جفت قلب در حلقههای 11 - 7 دیده میشود. از حلقه 12 به طرف عقب ، هر حلقه دارای رگهای بند بند زوج است که رگهای طولی را به اندامهای گوناگون مربوط میسازد.
دستگاه تنفس
دستگاه تنفسی منظم در این کرمها موجود نیست. خون جاری اکسیژن را در مویرگهای نزدیک کوتیکول مرطوب در دیواره بدن ، دریافت کرده و CO2 پس میدهد. اکسیژن با هموگلوبین در پلاسما ترکیب شده به بافتهای مختلف حمل میشود.
دستگاه عصبی
در بالای حلق (حلقه 3) یک جفت گانگلیونهای مغزی با مغز وجود دارد. دو رابط از پیرامون حلق به گانگلیونهای زیر مری دو قطعهای کشیده میشود، به نام حلقه دور مری و از گانگلیونهای زیر مری طناب عصبی شکمی در طول کف حفره عمومی بدن تا حلقه مخرجی امتداد مییابد. چندین عصب نیز به پیش دهان و ناحیه دهانی متصل میگردد. طناب عصبی شکمی در هر حلقه دارای یک عقده بزرگ است و 3 جفت عصب جانبی از آن خارج میشود. طناب و عقدهها به صورت ساختمانهای جفت بوجود میآید، رشته اعصاب جانبی به عضلات ، سلولهای اپیدرمی ، نفریدیها ، کیسههای تار و سایر اندامها عصب میدهد.
دستگاه تولید مثل
کرم خاکی تک جنسی است و در هر کرم اندامهای جنسی نر و ماده در قسمت شکمی جای دارد. کرمهای خاکی در بیشتر سال ، تولید مثل میکنند، ولی حداکثر فعالیت تکثیری آنها در هوای گرم و مرطوب است. جفتگیری در شب صورت گرفته. دو کرم خود را از سوراخ بیرون کشیده، سطح شکمی قدامیشان را نزدیک هم میآورند، بطوری که انتهای قدامیشان در دو جفت مخالف هم قرار دارد. در هر کرم یک جفت شیار اسپرمی تشکیل میشود که در طول آنها تودههای اسپرم به منظور دخول در جایگاه اسپرمی دیگری عبور میکند. پس از این عمل ، کرمها از هم جدا میشوند. بنابراین عمل لقاح دو جانبه و متقابل است
رابطه کرم خاکی با انسان
کرمهای خاکی به عنوان طعمه در ماهیگیری مصرف عملی دارند. اثرات طویلالمدت کرمهای خاکی در طبیعت جنبههای عملی مشخصی دارد. از آنجا که خاک را سوراخ میکنند اثرات قابل توجهی در حاصلخیزی خاک دارند.
منبع
جهت مشاهده آزمایشات علوم پایه(ریاضی،فیزیک،زیست شناسی وزمین شناسی وشیمی) روی هر عنوان کلیک نمایید سپس آزمایش مربوطه را روی کامپیوترخود ذخیره وآن را اجرا نمایید. امیدوارم از این فعالیت نهایت استفاده را برده باشید.
عکس های آزمایشگاه جانورشناسی 1
رو گذاشتم شما می توانید دانلود کرده وآن را
extract نمائید.
دانشجویان عزیز عکس های آزمایشگاه سلولی ومولکولی رو دانلود کنید
سپس از حالت فشرده خارج نمایید.
دانلود
این فایل ها گزارش كار آزمایشگاه شیمی آلی هست. امیدوارم بتونید ازشون استفاده كنید.
من قسمتی از گزارش كار (یعنی روش آزمایش ، نتایج ، خطا ها و خواص فیزیكی مواد) رو گذاشتم.
برای اجرای فایل ها اگر فرمت آنها PDF باشد با نرم افزار Acrobat Reader
میتونید اونها رو اجرا کنید.
اگر احیانا از شما نام کاربری و کلمه عبور میخواست ازینها استفاده کنید
نام کاربری : Shimi33
کلمه عبور : shimi22
- گزارش کار آزمایش تعیین نقطه ذوب دانلود
- گزارش کار آزمایش تقطیر 1 دانلود
- گزارش کار آزمایش تقطیر 2 دانلود
- گزارش کار آزمایش تقطیر بصورت کلی دانلود
- گزارش کار آزمایش تبلور دانلود --- دانلود۲
- گزارش کار آزمایش صابون دانلود
- گزارش کار آزمایش استرفیكاسیون دانلود
- آزمایش كروماتوگرافی
- گزارش کار آزمایش استخراج دانلود
- گزارش کار آزمایش ایزومریزاسیون
- گزارش کار آزمایش تصعید (تبلور مجدد)دانلود
- گزارش کار آزمایش سنتز آسپرین دانلود
- گزارش کار آزمایش ایزومری مالئیک اسید و فوماریک اسید دانلود
-
منبع http://organiclabzmm.blogfa.com/post-17.aspx
هدف :
1_ جدا سازی محصول اصلی یا محصول یا محصولات فرعی در یک واکنش شیمیایی :
در قدیم بهترین روش سنتز (که متنوع نبود ) در فاز مایع بود اما جدیدا در فاز جامد است و نیازمند استخراج است .
در فاز جامد از یک بستر پلیمری استفاده می کنیم ، ماده ای را که می خواهیم به بستر پلیمر متصل شود، به عنوان مثال A را به پلیمر متصل می کنیم بعد B را با آن واکنش می دهیم ، C و D ( محصولات ) چسبیده به پلیمر تشکیل می شوند ، وقتی پلیمر را می شوییم اگر A و B اضافی در محیط باشد خارج می شود ، می توانیم برای شست و شو از حلال های مختلفی استفاده کنیم چون با پلیمر واکنش نمی دهد .(سنتز در فار جامد : برای مواد آلی پیچیده )
و اما ادامه ی مطلب : A و B را که به عنوان واکنش دهنده وارد ترکیب کرده ایم بخشی مواد آلی و بخشی ترکیبات معدنی هستند ، ( فرض : ترکیبات معدنی در آب حل می شوند ) این مجموعه را چند بار شست و شو می دهیم تا فاز آلی و آبی جدا شود به شرطی که از ماده ی اصلی با آب ترکیب نشود که اگر ترکیب شود باید حلالیت را کاهش دهیم ( باید حلالیت ماده ی آلی را در فاز آبی تغییر دهیم یعنی Ksp را کاهش دهیم ، برای آن از نمک ها استفاده می کنند یعنی به جای آب محلول نمک طعام با غلظت بالا تهیه کرده و حل می کنند ، حلالیت ترکیب آلی کاهش یافته رسوب می کند و می توان با صافی جدا کرد ) شرط این که عمل استخراج را با راندمان بالا انجام دهیم این است که حلالیت دومی که بعدا از آب انتخاب می کنیم (با آب اختلاط نشود )
+ صابون در محلول NaCL و آب رسوب می دهد .
استخراج : خارج کردن یک ماده از یک حلال آلی یا آبی و بردن آن به یک حلال آلی یا آبی دیگر و اجازه دهیم که فاز آلی و آبی از هم جدا شوند سپس خدمان آن ها را جدا کنیم و با تبخیر و تقطیر ماده ی مورد نظر را از حلال جدا کنیم .
2_ خالص سازی یک ترکیب آلی و جدا سازی آن از ناخالصی هایش :
حلالی را انتخاب می کنیم که A در آن خوب حل شود و B کمتر، در واقع B یک ناخالصی برای A به حساب آید ، و در حلال دیگر ناخالصی بیشتر حل شود و A کمتر (( به شرطی که این حلال ها باهم اختلاط ندهند )) .اکثر این روش ها به وسیله ی حلال های غیر فعال شیمیایی صورت می گیرد .
حلال غیر فعال شیمیایی : معمولا هیچ واکنشی با مواد انجام نمی دهند و فقط کمک می کنند به حل شدن فیزیکی ماده ی آلی
3_ جدا سازی ترکیبات آلی بوسیله ی حلال های فعال شیمیایی :
این دو ترکیب در آب حل نمی شوند و در حلال آلی مثل اتر حل می شوند .حال تکلیف چیست ؟ از حلال های غیر فعال شیمیایی نمی توانیم برای جداسازی دو ترکیب فوق استفاده کنیم ، بنابر این از حلال های فعال شیمیایی استفاده می کنیم ، باید کاری کنیم که یکی از این ترکیبات در آب حل نشود .
حلال های فعال شیمیایی : اسیدها و باز ها و محلول های نمکی یا نمک ها
بنزیلات سدیم در آب حل می شود ، پس کافی است روی ترکیبات آب بریزیم که مرزی ایجاد خواهد شد، این مرز ها را جدا می کنیم ، آنیلین را جدا کرده و به سراغ بنزیلات سدیم می رویم که ماهیت ترکیب اولیه را عوض کرده ایم و باید بازش گردانیم برای این کار مقداری اسید اضافه می کنیم واکنش بر می گردد و بنزوئیک اسید رسوب می دهد .
آمین های آروماتیک در آب حل نمی شوند ، برای حل کردن آن به محیط اسید HCL اضافه می کنیم ، NH2 با +H حل شده ایجاد می شود ، برای برگشت آنیلین به حالت اولیه ی خودش به محیط -OH اضافه می کنیم .
گاهی اوقات محلول نمکی ماهیت ترکیب را تغییر می دهد و Ksp آن را هم در آب افزایش میدهد .
روش های استخراج : 1_ مایع _ مایع 2_ جامد _ مایع
مایع _ مایع :شکل فیزیکی هر دو ماده مایع است ، حلالی هم که استفاده می کنیم مایع است .
حلالی را انتخاب می کنیم که یکی از مواد مثل A در آن بیشتر حل شود و B کمتر و حلال دیگری برعکس باشد اما اگر هر دو ماده ی A و B در حلال حل شوند عیبی ندارد می شود روش استخراج را عوض کرد یعنی حلالیت یکی را کم کنیم یعنی تغییر حلالیت دهیم .
رزولسینول ها بسیار خورنده هستند و سمی ، در داخل دی اتیل اتر بهتر حل می شود .
جامدی بدست می آوریم که ویسکوزیته ی بالا دارد چون نقطه ی ذوب آن پایین است . به محض این که حرارت دید مقداری جامد شده مجددا مایع می شود که ویسکوزیته ی بالا دارد ، در نهایت یک پودری بدست می آید (( پودر هموژن قهوه ای رنگ )) .
اگر رنگ متفاوت بود بدین معنی است که مقداری از حلال باقی مانده و باید خوب بهم بزنیم تا خارج شود .
طبقه بندی روش های استخراج از نظر تعداد دفعات استخراج :1_ پیوسته 2_ ناپیوسته .
در پیوسته یک بار حجم مشخصی از حلال را بر می داریم و در طول تمامی مراحلاستخراج با همان حجم مشخص کار می کنیم . در ناپیوسته هر بار که می خواهیم عمل استخراج را تکرار کنیم باید یک حجم جدیدی از حلال را بر داریم ،
استخراج پیوسته مقرون به صرفه است .
دستگاه سکسوله : استخراج پیوسته درون آن انجام می گیرد ، استخراج از نوع جامد_مایع
حلال ها: استون ، متانول ، اتانول، و یا مخلوط آب و استون_آب و متانول و آب و اتانول
از این این مخلوط های حلال ها استفاده می کنند چون دمای جوش آب بالا و دمای جوش بقیه پایین است در اثر حرارت دادن ترکیبات آلی آسیب نبینند .
فشار با نقطه ی جوش رابطه ی مستقیم دارد .
خصوصیت حلال های مناسب غیر فعال شیمیایی :
1_ به آسانی قابل جدا کردن باشد 2_ با ماده ی آل واکنش شیمیایی ندهد 3_ سمس و آتش گیر نباشد و ارزان باشد 4_ ماده ی ناخالصی تا حد امکان داخل حلال کمتر حل شود
البته اکثر حلال ها سمی و آتش گیر هستند که برای جبران آن ها از مخلوط حلال ها استفاده می کنیم .
ضریب توزیع :
وقتی می خواهیم ضریب توضیع A را داخل دو حلال 1 و 2 بدست آوریم :
k= غلظت ماده ی A داخل فاز 2 / غلظت ماده ی A داخل فاز 1
K>>1 : یعنی با یک یا دو بار استخراج ماده A را به طور کمی از فاز 1 به فاز 2 می بریم
K<<1 : باید تعداد دفعات استخراج را بیشتر کنیم تا ماده ی A را به طور کمی از فاز 1 به فاز 2 ببریم
تنها عامل فیزیکی که در ضریب توزیع تاثیر می گذارد دما است : دما بیشتر ضریب توزیع بیشتر.
منبع:سایت علمی نخبگان جوان
آلکانها، هیدروکربنهایی هستند که در آنها هر اتم کربن با ۴ پیوند به ۴ اتم هیدروژن یا کربن میچسبند. در واقع پیوند دو یا سه گانه بین اتمهای کربن وجود ندارد. فرمول کلی آلکانها CnH۲n+۲ است. سادهترین آلکان، متان (CH۴) است که بخش عمده گاز طبیعی را تشکیل میدهد. اتان (C۲H۶)، پروپان (C۳H۸) و بوتان (C۴H۱۰) دیگر آلکانهای گازی هستند. پنتان (C۵H۱۲)، هگزان (C۶H۱۴)، هپتان (C۷H۱۶) و اکتان (C۸H۱۸) مهمترین آلکانهای مایع هستند.
نامگذاری آلکانها را موسسه آیوپاک انجام میدهد.
تعداد ایزومرها به ترتیب ۱، ۱. ۱، ۲، ۳، ۵، ۹، ۱۸، ۳۵، ۷۵، ۱۵۹، ۳۵۵،....
تا به حال فرمولی برای تعداد آلکانها پیدا نشده است . فرمول زیر برای آلکانهایی است که دارای ۴ تا ۷ کربن هستند. 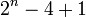
آلکانها میتوانند راست زنجیر یا شاخه دار باشند . مولکولهایی که فرم مولکولی یکسان دارند، اما آرایش اتمها در آنها متفاوت است . هم پاریاایزومر مینامند . آلکانهایی که چهار یا تعداد بیش تری اتم کربن داشته باشند دارای ایزومر هستند . همهٔ آلکانها، گازها، مایعها یا جامدهایی بی رنگ هستند که با افزایش اعداد کربن نقطه جوش و گرانوری(گرانوری یک مایع،میزان عدم تعادل آن رابرای جاری شدن معین می کند) آنها افزایش مییابد . همهٔ آلکانها در هوا با شعله زرد – آبی تمیزی میسوزند .
خواص فیزیکی آلکانها از همان الگوی خواص فیزیکی متان پیروی میکند و با ساختار آلکانها سازگار است. یک مولکول آلکان فقط بهوسیله پیوندهای کووالانسی برپا نگه داشته شدهاست. این پیوندها یا دو اتم از یک نوع را بهم متصل میکنند و در نتیجه، غیر قطبیاند، یا دو اتم را که تفاوت الکترونگاتیوی آنها بسیار کم است، به یکدیگر ربط میدهند و در نتیجه قطبیت آنها کم است. به علاوه، این پیوندها به طریقی بسیار متقارن جهت گرفتهاند، بطوری که این قطبیهای پیوندی نیز یکدیگر را خنثی میکنند.
در نتیجه یک مولکول آلکان یا غیر قطبی است یا قطبیت بسیار ضعیفی دارد. نیروهایی که مولکولهای غیر قطبی را گرد هم نگه میدارند (نیروهای واندروالسی) ضعیف هستند و گستره بسیار محدودی دارند. این نیروها فقط بین بخشهایی از مولکولهای مختلف که با یکدیگر در تماس نزدیک باشند، یعنی بین سطوح مولکولها، عمل میکنند. بنابراین در یک خانوداه معین، انتظار داریم که هر اندازه مولکول بزرگتر و شود در نتیجه سطح تماس آنها بیشتر شود، نیروهای بین مولکولی نیز قویتر میشوند.
دمای جوش و ذوب با افزایش شمار اتمهای کربن، زیاد میشود. فرایند جوشیدن و ذوب شدن، مستلزم فایق آمدن بر نیروهای بین مولکولی در یک مایع و یک جامد است. دمای جوش و دمای ذوب بالا میرود، زیرا این نیروهای بین مولکولی با بزرگ شدن مولکولها افزایش مییابند.
منبع:ویکی پدیا
مقدمه:
واکنش دیلز –آلدر واکنشی است که در آن یک آلکن با یک دی ان مزدوج (۱و۳-دی ان) واکنش می دهد و مشتقی از سیکلو هگزن ایجاد می کند.به آلکن معمولا دی ان دوست یا دی انوفیل می گویند.واکنش اتیلن با بوتا دی ان منجر به تشکیل سیکلو هگزن می شود.
واکنش دیلز – آلدر یکی از مهمترین روش های سنتزی است که در دسترس شیمیدانان آلی است.چنانچه بجای آلکن از یک آلکین استفاده شود مشتقی از ۱ و ۴- سیکلوهگزا دی ان بدست می آید.
واکنش دیلز – آلدر روشی بسیار مناسب برای تشکیل پیوند کربن – کربن و ترکیبات حلقوی شش ضلعی می باشد.در این واکنش پیوندهای کربن –کربن دارای پیوند π در دی انوفیل ازیک طرف و کربنهای ۱ و ۴ – دی ان از طرف دیگر تشکیل می شود بنابراین روی هم رفته دی انوفیل به صورت ۱ و ۴ به دی ان افزایش می یابد.بنابراین پیوندهای دوگانه مزدوج علاوه بر واکنش های معمولی آلکنها مانند افزایش الکترون دوستی در واکنشی دیگر یعنی واکنش دیلز – آلدر نیز شرکت می کنند.این تبدیل که به حلقه افزایی دیلز –آلدر معروف است پیوندهای جدید همزمان و به صورت فضا ویژه تشکیل می شوند. با توجه به اینکه ایجاد کربنهای کایرال امری نه چندان آسان در سنتزهای آلی می باشند، توانایی این واکنش در تشکیل راحت ترکیبات با مراکز نامتقارن اهمیت این دسته از واکنش ها را دو چندان می نماید. از جمله دی انهای مورد استفاده در کاربردهای واکنش دیلز – آلدر ترکیبات حلقوی سولفوردار می باشد. در سالهای اخیر مطالعات زیادی روی ترکیبات حلقوی سولفوردار جهت سنتز ترکیبات مختلف شده است. در این میان ترکیبات حلقوی سولفوردار H 2- تیوپیران -۴- اًُن از اهمیت خاصی برخوردار می باشند. اهمیت این ترکیبات از آنجا ناشی می شود که با استفاده از واکنش دیلز – آلدر این ترکیبات می توان بر محدودیت اساسی واکنش های دیلز – آلدر یعنی واکنش پذیری کم یا عدم واکنش پذیری دی انهای سیس غلبه نمود. دی انهای سیس اغلب هیچ محصول افزایشی در واکنش با دی انوفیلها تولید نمی کنند ولی در عوض دی انهای ترانس هزار برابر فعالتر از دی انهای مشابه سیس می باشند. این عدم واکنش پذیری مربوط به ازدحام فضایی موجود در دی انهای سیس می باشد. یک استراتژی مناسب جهت فائق آمدن بر این مشکل، استفاده ازH 2- تیوپیران -۴- ان می باشد. اولین بار گروه پروفسور Ward و همکارانش از کانادا موفق به انجام واکنش های دیلز – آلدر با استفاده از این ترکیبات به عنوان جانشینان مناسب دی انهای سیس شدند.
این گروه با انجام واکنش دیلز – آلدر بین دی هیدروتیوپیران -۴-ان با دی انوفیلهای خاص و در ادامه سولفورزدایی محصولات، موفق به شناسایی محصولاتی شدند که هم ارز با محصولات دیلز – آلدر حاصل از دی انهای سیس که توانایی شرکت در واکنش دیلز – آلدر را نداشتند، می باشند. با توجه به اهمیت این واکنشها، بر آن شدیم که در این پژوهش به ادامه مطالعات بپردازیم و سنتز ترکیبات جدیدی از این نوع را انجام دهیم.
شرح آزمایش:
در یک بالن تقطیر کاملا خشک حدود ۳ گرم آنتراسن .۲ گرم مالئیک انهایدراید و ۲۰ میلی لیتر تولوئن می ریزیم و ۲ عدد سنگ جوش اضافه کرده ۴۰ دقیقه رلکس می کنیم.پس از خنک شدن محتویات بالن رسوب حاصل را صاف می کنیم بعد از خشک شدن رسوب راندمان را محاسبه می کنیم
عنوان آزمایش: خالص سازی مواد به روش استخراج
هدف: استخراج آدیپیک اسید از فاز آبی به فاز آلی(اتر)
تئوری آزمایش:
استخراج روشی است برای جداسازی که در آن جسمی از یک فاز به فاز دیگر منتقل می شود. در بعضی مواقع لازم است برای بازیابی یک ماده آلی از راههایی غیر از تقطیر استفاده شود. یکی از این راهها تماس دادن محلول آبی با یک حلال غیر قابل اختلاط با آب است. اگر حلال مناسب باشد، بیشتر مواد آلی(در اینجا آدیپیک اسید) از لایه آبی به حلال آلی (که با آب امتزاج ناپذیر است) انتقال پیدا میکند.
از نظر کمی پخش یک جسم بین دو حلال غیر قابل امتزاج را بر حسب ضریب پخش K بیان میکنند. به عبارت دیگر ضریب پخش(k) یعنی: نسبت غلظت ماده ی حل شده در حلال اول، به غلظت همان ماده در حلال دوم.
حلالی که برای استخراج انتخاب می شود باید دارای این ویژگیها باشد:
1- با حلالی که دارای ماده مورد نظر است،مخلوط نشود.(سیستم دو فازی تشکیل دهد)
2- K ماده در حلال انتخاب شده بزرگ باشد. (یعنی ماده در حلال دوم بیشتر از حلال اول محلول باشد)
3- حلال نباید ما ماده مورد نظر واکنش دهد.
4- حلال انتخاب شده به آسانی تبخیر شود.
5- حلال نباید ناخالصی ها را استخراج کند.
در استخراج مایع-مایع از قیف جدا کننده (دکانتور) استفاده می شود.قیف نباید بیشتر از سه چهارم حجم آن پر شود چون در این صورت امکان هم زدن محلول وجود نخواهد داشت.هدف از تکان دادن و هم زدن این است که سطح تماس دو حلال افزایش یابد و ماده حل شده در حلال اول در مدت زمان کمتری بتواند به حلال دوم برود.(در آن حل شود).هر چند ثانیه یک بار باید قیف را برگرداند(شیر به سمت بالا) و آن را به آرامی باز کرد تا گاز قیف خارج شود.این عمل همیشه باید انجام شود ولی در دو حالت اهمیت بیشتری دارد:
1- وقتی که حلال مورد استفاده دمای جوش پایینی داشته باشد.
2- یک محلول اسیدی با محلولی از سدیم بیکربنات استخراج شود.(در این حالت گاز کربن دی اکسید آزاد می شود)
پس از تکان دادن قیف و خارج کردن گازهای آن، قیف جدا کننده را روی گیره ی حلقه ای قرار می دهند و فرصت می دهند تا فازها به خوبی از هم جدا شوند.
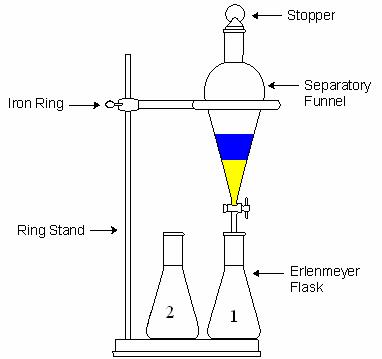
لایه ها طوری جدا می شوند که حلال سنگین تر در پایین قرار می گیرد اما گاهی ممکن است به دلیل حل شدن بیشتر ماده در فاز آلی، حلال آلی پایین تر از آبی قرار بگیرد.برای اطمینان از اینکه کدام فاز آلی و کدام آبی است،در یک بشر کوچک مقداری آب ریخته و سپس با باز کردن شیر قیف جدا کننده چند میلی لیتر از حلال پایینی را به بشری که در آن آب ریخته ایم اضافه می کنیم،اگر دو محلول در یکدیگر حل شوند فاز پایینی آبی است و در غیر اینصورت آلی است.
وسایل و مواد لازم:
آدیپیک اسید، سدیم هیدروکسید، محلول فنل فتالئین، دی اتیل اتر، آب مقطر
قیف جدا کننده، بورت، بشر، همزن، قطره چکان، ارلن،
روش کار:
حلال اول در این ازمایش آب و حلال دوم اتر است.ماده مورد نظر هم آدیپیک اسید می باشد.در این ازمایش میخواهیم آدیپیک اسید را که در آب محلول است،توسط اتر استخراج و به فاز آلی ببریم.
1 گرم آدیپیک اسید را در 100 سی سی آب مقطر حل می کنیم.(همان محلول 1% ).
(از این قسمت می توان غلظت آدیپیک اسید را در فاز آبی حساب کرد.به این صورت که با توجه به وزن آدیپیک اسید و جرم مولکولی آن تعداد مول را حساب کرده و تقسیم بر حجم محلول کنیم.
علاوه بر این می توان بصورت عملی نیز غلظت را در موارد مجهول با استفاده از تیتراسیون با یک محلول باز حساب کرد.)
25 سی سی از این محلول را در قیف جدا کننده می ریزیم و به آن 30 سی سی اتر اضافه می کنیم.عمل استخراج را با توجه به نکات عملی گفته شده انجام می دهیم و سپس مدتی قیف را روی حلقه ساکن می گذاریم تا دو فاز از هم جدا شوند.و هر فاز را بصورت جداگانه داخل ارلن می ریزیم.
در این حالت و پس از انجام عمل استخراج،آدیپیک اسید که در فاز آبی بود به فاز اتری(آلی) منتقل می شود.اما برای اینکه بدانیم چه مقدار از آدیپیک اسید به فاز آلی منتقل شده است، محلول اتری به دست آمده از عمل استخراج را،با محلول سدیم هیدروکسید تیتر می کنیم.
M1 مولاریته اسید در فاز آلی
V1 حجم فاز آلی
M2 مولاریته محلول سدیم هیدروکسید ( این محلول را خودمان تهیه می کنیم پس مقدار مولاریته ی آن را می توانیم با توجه به جرمی از سود که در مقدار مشخصی آب حل کرده ایم حساب کنیم)
V2 حجم محلول سدیم هیدروکسید مصرف شده (در تیتراسیون)
(چون آدیپیک اسید یک اسید دو عاملی است حتماً باید موقع محاسبه غلظت بعد از انجام تیتراسیون ضریب دو را نیز در فرمول فوق واردکنیم.)
به این ترتیب می توان مولاریته اسید در فاز آلی یعنی M1 را بدست آورد.و به این ترتیب متوجه می شویم که چه مقدار از اسید از فاز آبی به فاز آلی منتقل شده است.و در این حالت K به آسانی قابل محاسبه خواهد بود.
مثلاً اگر مولاریته با انجام تیتراسیون 0.5 مولار بدست اید.در این حالت K به این صورت خواهد بود:
مفهوم این عدد این است که ماده مورد نظر در حلال دوم(اتر) 2.77 برابر حلال اول(آب) حل می شود.
در پایان می توان به این سوالات پاسخ داد:
1- وزن اسید در لایه ی اتری و آبی چقدر است؟
راهنمایی: مولاریته اسید در هر دو فاز را بدست آوردیم.برای به دست آوردن وزن اسید در هر لایه کافیست به حجم برداشته شده از دو حلال دقت کنیم. یعنی با داشتن مولاریته و حجم به راحتی تعداد مول را بدست آورده و تعدا مول را با استفاده از جرم مولکولی اسید،به وزن(جرم) تبدیل کنیم.
2- درصد اسید در لایه ی اتری و آبی چقدر است؟
راهنمایی: پس از بدست اوردن جواب سوال اول، می توان درصد وزنی وزنی را نیز حساب کرد. مثلا اگر وزن ترکیب در 25 سی سی 2 گرم باشد،بدیهی است که در صد سی سی 8 خواهد بود(8درصد)
3- بازده استخراج چقدر است؟
راهنمایی: در حالت ایده آل (یعنی بازده 100%) باید کل اسید از فاز آبی به آلی منتقل شود که مطمئناً این گونه نیست.و مقداری از اسید در آب باقی خواهد ماند.بازده را در اینجا می توان برحسب غلظت یا وزن حساب کرد.(که جوابها یکی است)
بازده= مقدار استخراج شده ی اسید تقسیم بر مقدار اولیه اسید
4- غلظت کل اسید داده شده در مجهول اولیه چقدر بوده است؟
غلظت اولیه اسید در بالا در متن روش کار حساب شد. و یا می توانستیم از طریق تیتراسیون محاسبه کنیم.
5- K را محاسبه کنید.
مقدار فرضی k در بالا حساب شد. به همان روش می توان مقدار k را در آزمایش حساب کرد.
در پایان آزمایش باید نتیجه گیری و منابع خطا ذکر شود.
* جدول خصوصیات آدیپیک اسید جهت اطلاع بیشتر:
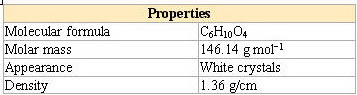
جزوه آزمایشگاه میکروبیولوژی عمومی تهیه شده توسط مهرنوش تنگستانی
فهرست مطالب:
اصول اولیه کار در آزمایشگاه میکروبیولوژی
آشنایی با وسایل و ابزار کار با آزمایشگاه میکروب شناسی
استریلیزاسیون در آزمایشگاه
استریلیزاسیون توس دستگاه اتوکلاو
محیط های کشت باکتریایی
انواع تقسیم بندی محیط های کشت
آماده سازی و استریل کردن محیط های کشت میکروبی
کشت باکتری
تهیه رقت یا رقیق کردن نمونه (Serial Dilution)
آزمایش مستقیم نمونه ها
رنگ آمیزی گرم Gram Staining
رنگ آمیزی کپوسل (رنگ آمیزی منفی یا زمینه سیاه)
رنگ آمیزی اسیدفاست (روش زیل نیلسون)
رنگ آمیزی اسپور
رنگ آمیزی کپکها
دانلود جزوه

پاورپوینت آزمایشگاه سیستماتیک گیاهی 2، بخش دوم
درس آزمایشگاه سیستماتیک گیاهی 2، یکی از واحد های تئوری و عملی اصلی رشته ی زیست شناسی (زیست شناسی گیاهی، جانوری و دریا)در مقطع کارشناسی می باشد. روند اصلیِ گذراندن واحد عملی این درس آشنایی با نمونه های هرباریومی گیاهی است که جهت آشنایی دانشجویان با طبقه بندی گیاهان صورت می گیرد. نمونه گیاهانی که دانشجویان در این درس با آنها آشنا می شوند شامل 6 زیررده (زیررده ماگنولیوئیده، هاملیده، کاریوفیلیده، رزیده،دیله نئیده،آستریده) از گیاهان دولپه ای می باشد. در این واحد عملی دانشجویان با مشاهده ی نمونه های هرباریومی و یا نمونه های زنده در طبیعت با ساختار کلی گیاهان و ویژگی های خاصی که جهت شناسایی آنها به کار می رود، آشنا شده و در نهایت با رسم تصویر گیاه و جزئیات ساختاری آن گزارش کار مربوط به هر جلسه را تهیه و تنظیم می کنند. تعداد استاندارد نمونه های گیاهی که در واحد عملی سیستماتیک گیاهی2، مشاهده و بررسی می شود 60-50 نمونه بوده و در تمامی دانشگاه ها (سراسری، پیام نور، آزاد، علمی کاربردی ) تقریباً یکسان است. پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2 در 7 بخش تهیه و تنطیم شده که شامل تصاویر تمامی جنس های مهم گیاهان دو لپه ای می باشد. تهیه و تنظیم این فایل به منظور آشنایی دانشجویان و همچنین سایر افرادی که علاقه مند به شناسایی و مطالعه ی گیاهان هستند، صورت گرفته است.
در اینجا جزوه پاورپویینت درس آزمایشگاه سیستماتیک گیاهی 2 بخش دوم در 58 صفحه برای شما عزیزان قرار داده شده است.
لینک دانلود مستقیم فایل در 58 صفحه
حجم فایل: 12.0 مگابایت

پاورپوینت آزمایشگاه سیستماتیک گیاهی 2، بخش سوم
رده دولپهایها/ نهاندانگان دولپه
نهاندانگان دولپه، گروهی از گیاهان هستند که از تکامل بازدانگان بوجود آمدهاند. دانه در این گروه از دانه گیاهان تکلپهای در وضع رشد جنین که به سرعت متوقف شده و دو نقطه جانبی آن بر اثر رشد ایجاد دو لپه متورم را میکند متفاوت بوده و همچنین ریشه اصلی در دولپهایها از رشد ریشهچه جنین ایجاد میشود. ساقه و ریشه دارای ساختار پسین و رشد قطری است. در این گروه گیاهان زیادی قرار دارند. از جمله تیره حبوبات ، تیره بنفشه ، تیره شب بو ، تیره گل مینا ، تیره میخک ، تیره زیتون و...
• دو لپهایها خود شامل دو لپهایهای بیگلبرگ ، دو لپهایهای جدا گلبرگ و دو لپهایهای پیوسته گلبرگ میباشد که تعداد زیادی از گیاهان دانهدار را در خود جای دادهاند.
درس آزمایشگاه سیستماتیک گیاهی 2، یکی از واحد های تئوری و عملی اصلی رشته ی زیست شناسی (زیست شناسی گیاهی، جانوری و دریا)در مقطع کارشناسی می باشد. روند اصلیِ گذراندن واحد عملی این درس آشنایی با نمونه های هرباریومی گیاهی است که جهت آشنایی دانشجویان با طبقه بندی گیاهان صورت می گیرد. نمونه گیاهانی که دانشجویان در این درس با آنها آشنا می شوند شامل 6 زیررده (زیررده ماگنولیوئیده، هاملیده، کاریوفیلیده، رزیده،دیله نئیده،آستریده) از گیاهان دولپه ای می باشد. در این واحد عملی دانشجویان با مشاهده ی نمونه های هرباریومی و یا نمونه های زنده در طبیعت با ساختار کلی گیاهان و ویژگی های خاصی که جهت شناسایی آنها به کار می رود، آشنا شده و در نهایت با رسم تصویر گیاه و جزئیات ساختاری آن گزارش کار مربوط به هر جلسه را تهیه و تنظیم می کنند. تعداد استاندارد نمونه های گیاهی که در واحد عملی سیستماتیک گیاهی2، مشاهده و بررسی می شود 60-50 نمونه بوده و در تمامی دانشگاه ها (سراسری، پیام نور، آزاد، علمی کاربردی ) تقریباً یکسان است. پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2 در 7 بخش تهیه و تنطیم شده که شامل تصاویر تمامی جنس های مهم گیاهان دو لپه ای می باشد. تهیه و تنظیم این فایل به منظور آشنایی دانشجویان و همچنین سایر افرادی که علاقه مند به شناسایی و مطالعه ی گیاهان هستند، صورت گرفته است.
در اینجا جزوه پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2، بخش سوم، در 50 صفحه برای شما عزیزان قرار داده شده است.
لینک دانلود مستقیم فایل در 50 صفحه
حجم فایل: 8.5 مگابایت

پاورپوینت آزمایشگاه سیستماتیک گیاهی 2، بخش چهارم
رده بندی نهاندانگان
در زیست شناسی به روند قرار دادن گیاهان در گروهها که دارای رابطه هایی با یکدیگر هستند، رده بندی اطلاق میشود. دو لپهایها ردهای از زیر شاخه نهاندانگان هستند که خود به زیر ردههایی قابل تقسیم هستند.قرائن و مدارک موجود نشان میدهد که گیاهان نهاندانه امروزی به احتمال قوی از تحول تدریجی و تکامل گیاهان پستتر بوجود آمدهاند و این تکامل همچنان ادامه دارد. بنابراین انواع نهاندانگان کنونی دارای اجداد مشترک بوده و در نتیجه با هم خویشاوندند. برای رده بندی گیاهان روش بسی را که بیشتر نظر گیاه شناسان را جلب میکند، مورد توجه قرار میدهند. در روش بسی ، رده رانال نخستین گروه گیاه نهاندانه است. دو تیره اولیه آن ، تیرههای ماگنولیا و آلاله است. تیره ماگنولیا ابتداییتر و تیره آلاله تکامل یافتهتر است. اگر چه هر دو رده تیره گل دارند و صفات مشترک بسیار دارند، ولی گیاهان تیره ماگنولیا بیشتر به صورت درخت و درختچه و گیاهان تیره آلاله بیشتر علفیاند. دیرین گیاه شناسی معلوم داشته است که درخت زودتر از علف بوجود آمده است. بنابراین گیاهان تیره ماگنولیا میبایست زودتر از گیاهان تیره آلاله بوجود آمده باشند. طبق نظریه بسی گلهای ابتدایی نوع رانال که نمونه آن ماگنولیا و آلاله است، دست کم در سه مسیر تکامل یافتهاند. این مسیرها به پیدایش گیاهان تیرههای نعناع ، مینا ، ثعلب انجامیدهاند.ویژگی بارز آنتوفیتها در این است که تخمکهای آنها درون تخمدان بسته نهفتهاند. این گیاهان اغلب در خشکی میرویند. بعضی از نهاندانگان با اینکه فتوسنتز میکنند، ولی فاقد ریشهاند و آب و مواد کانی لازم را از میزبان خود تامین میکنند. برخی نیز فاقد کلروفیل میباشند و زندگی انگلی دارند. معدودی مانند عدسک آبی ، کوچک و ظریف و بدون ساقه در سطح آب شناورند. عدهای علفی یا به صورت درختچه یا درختاند. ساختار ساقه آنها بر حسب محیط زیست متفاوت است. مثلا کاکتوس ، ساقهای گوشتی و برگهایی خارمانند دارد و با این ویژگیها میتواند در شرایط نامناسب خشک و گرم بیابان زندگی کند.نهاندانگان در حدود 130 تا 140 میلیون سال پیش ظاهر شدهاند.
• رده دولپهایها
این گروه گیاهی از تکامل بازدانگان بوجود آمدهاند. دانه در این گروه از دانه گیاهان تکلپهای در وضع رشد جنین که به سرعت متوقف شده و دو نقطه جانبی آن بر اثر رشد ایجاد دو لپه متورم را میکند متفاوت بوده و همچنین ریشه اصلی در دولپهایها از رشد ریشهچه جنین ایجاد میشود. ساقه و ریشه دارای ساختار پسین و رشد قطری است. در این گروه گیاهان زیادی قرار دارند. از جمله تیره حبوبات ، تیره بنفشه ، تیره شب بو ، تیره گل مینا ، تیره میخک ، تیره زیتون و...
• دو لپهایها خود شامل دو لپهایهای بیگلبرگ ، دو لپهایهای جدا گلبرگ و دو لپهایهای پیوسته گلبرگ میباشد که تعداد زیادی از گیاهان دانهدار را در خود جای دادهاند.
درس آزمایشگاه سیستماتیک گیاهی 2، یکی از واحد های تئوری و عملی اصلی رشته ی زیست شناسی (زیست شناسی گیاهی، جانوری و دریا)در مقطع کارشناسی می باشد. روند اصلیِ گذراندن واحد عملی این درس آشنایی با نمونه های هرباریومی گیاهی است که جهت آشنایی دانشجویان با طبقه بندی گیاهان صورت می گیرد. نمونه گیاهانی که دانشجویان در این درس با آنها آشنا می شوند شامل 6 زیررده (زیررده ماگنولیوئیده، هاملیده، کاریوفیلیده، رزیده،دیله نئیده،آستریده) از گیاهان دولپه ای می باشد. در این واحد عملی دانشجویان با مشاهده ی نمونه های هرباریومی و یا نمونه های زنده در طبیعت با ساختار کلی گیاهان و ویژگی های خاصی که جهت شناسایی آنها به کار می رود، آشنا شده و در نهایت با رسم تصویر گیاه و جزئیات ساختاری آن گزارش کار مربوط به هر جلسه را تهیه و تنظیم می کنند. تعداد استاندارد نمونه های گیاهی که در واحد عملی سیستماتیک گیاهی2، مشاهده و بررسی می شود 60-50 نمونه بوده و در تمامی دانشگاه ها (سراسری، پیام نور، آزاد، علمی کاربردی ) تقریباً یکسان است. پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2 در 7 بخش تهیه و تنطیم شده که شامل تصاویر تمامی جنس های مهم گیاهان دو لپه ای می باشد. تهیه و تنظیم این فایل به منظور آشنایی دانشجویان و همچنین سایر افرادی که علاقه مند به شناسایی و مطالعه ی گیاهان هستند، صورت گرفته است.
در اینجا جزوه پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2، بخش چهارم، در 44 صفحه برای شما عزیزان قرار داده شده است.
لینک دانلود مستقیم فایل در 44 صفحه
حجم فایل: 7.26 مگابایت

پاورپوینت آزمایشگاه سیستماتیک گیاهی 2، بخش پنجم
• رده دولپهایها
نهاندانگان دولپه از تکامل بازدانگان بوجود آمدهاند. دانه در این گروه از دانه گیاهان تکلپهای در وضع رشد جنین که به سرعت متوقف شده و دو نقطه جانبی آن بر اثر رشد ایجاد دو لپه متورم را میکند متفاوت بوده و همچنین ریشه اصلی در دولپهایها از رشد ریشهچه جنین ایجاد میشود. ساقه و ریشه دارای ساختار پسین و رشد قطری است. در این گروه گیاهان زیادی قرار دارند. از جمله تیره حبوبات ، تیره بنفشه ، تیره شب بو ، تیره گل مینا ، تیره میخک ، تیره زیتون و...
• دو لپهایها خود شامل دو لپهایهای بیگلبرگ ، دو لپهایهای جدا گلبرگ و دو لپهایهای پیوسته گلبرگ میباشد که تعداد زیادی از گیاهان دانهدار را در خود جای دادهاند.
درس آزمایشگاه سیستماتیک گیاهی 2، یکی از واحد های تئوری و عملی اصلی رشته ی زیست شناسی (زیست شناسی گیاهی، جانوری و دریا)در مقطع کارشناسی می باشد. روند اصلیِ گذراندن واحد عملی این درس آشنایی با نمونه های هرباریومی گیاهی است که جهت آشنایی دانشجویان با طبقه بندی گیاهان صورت می گیرد. نمونه گیاهانی که دانشجویان در این درس با آنها آشنا می شوند شامل 6 زیررده (زیررده ماگنولیوئیده، هاملیده، کاریوفیلیده، رزیده،دیله نئیده،آستریده) از گیاهان دولپه ای می باشد. در این واحد عملی دانشجویان با مشاهده ی نمونه های هرباریومی و یا نمونه های زنده در طبیعت با ساختار کلی گیاهان و ویژگی های خاصی که جهت شناسایی آنها به کار می رود، آشنا شده و در نهایت با رسم تصویر گیاه و جزئیات ساختاری آن گزارش کار مربوط به هر جلسه را تهیه و تنظیم می کنند. تعداد استاندارد نمونه های گیاهی که در واحد عملی سیستماتیک گیاهی2 ، مشاهده و بررسی می شود 60-50 نمونه بوده و در تمامی دانشگاه ها (سراسری، پیام نور، آزاد، علمی کاربردی ) تقریباً یکسان است. پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2 در 6 بخش تهیه و تنطیم شده که شامل تصاویر تمامی جنس های مهم گیاهان دو لپه ای می باشد. تهیه و تنظیم این فایل به منظور آشنایی دانشجویان و همچنین سایر افرادی که علاقه مند به شناسایی و مطالعه ی گیاهان هستند، صورت گرفته است.
در اینجا جزوه پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2، بخش پنجم، در 40 صفحه برای شما عزیزان قرار داده شده است.
لینک دانلود مستقیم فایل در 40 صفحه
حجم فایل: 5.46 مگابایت

پاورپوینت آزمایشگاه سیستماتیک گیاهی 2، بخش هفتم
زیر شاخه نهاندانگان شامل دو رده تک لپه ایها و دو لپه ایها می باشد. دو لپه ایها خود شامل دو لپه ایهای بی گلبرگ ، دو لپه ایهای جدا گلبرگ و دو لپه ایهای پیوسته گلبرگ می باشد که تعداد زیادی از گیاهان دانه دار را در خود جای داده اند.
دو لپه ایهای جدا گلبرگ Dialypetalae
گیاهانی هستند با گلهای کامل و دو جنسه که پوشش گل آنها به صورت کاسبرگ و گلبرگ تمایز یافته و اجزای گل در چرخه های متوالی و به صورت متناوب باهم قرار دارند و گرده افشانی در آنها بوسیله حشرات صورت می گیرد. جدا گلبرگها بالغ بر ۷۰ هزار گونه گیاهی هستند و براساس ساختمان نهنج و نحوه قرار گرفتن اجزای گل در سه گروه فرعی قرار می گیرند.
تالامیفلورها
که در آنها نهنج گل برآمده یا گنبدی شکل است و اجزای گل مستقیما بر روی نهنج استقرار یافته اند و شامل ۵ راسته است.
ـ راسته آلاله گان (Ranales):
که برچه ها جدا از هم و اجزای گل غالبا در روی یک خط مارپیچی در سطح نهنج قرار دارند.
ـ راسته پاریتال (parietals): که برچه ها پیوسته بهم و تمکن آنها جانبی است.
ـ راسته گوتیفرال (Gutti ferales):
که برچه ها پیوسته بهم و تمکن آنها محوری و کاسبرگها در داخل غنچه گل ، همپوشان هستند.
ـ راسته ختمی (Malvales):
که برچه ها پیوسته بهم و تمکن آنها محوری و کاسبرگها در داخل گل به صورت کفه ای قرار دارند.
ـ راسته فرفیون (Euphorbiales):
که برچه ها پیوسته بهم و تمکن آنها محوری ، گلها یک جنسه و غالبا فاقد گلبرگ هستند.
دیسیفلورها
که در آنها نهنج گل برآمده یا گنبدی شکل است و اجزای گل در سطح دستگاه مولد شهد و یا به حالت فررفته در آن قرار دارند.
ـ راسته شمعدانی (Geraniales):
نافه شامل دو ردیف پرچم و دستگاه ترشحی به صورت غده هایی در پای پرچمها قرار دارد.
ـ راسته افرا (Sapindales):
نافه شامل دو ردیف پرچم و دستگاه مولد شهد به صورت یک صفحه در محوطه خارجی پرچمها قرار دارند.
ـ راسته شمشاد (Celastrales):
نافه شامل یک ردیف پرچم و دستگاه مولد شهد در داخل پرچمها و خارج پرچمها قرار دارد.
کالسیفلورها
سه جزء خارجی اجزای گل یعنی کاسبرگها ، گلبرگها و پرچمها از قسمت زیرین خود بهم پیوسته اند و نهنج پیاله مانند یا کوزه ای شکل را در انتهای دمگل بوجود آورده اند. این گروه شامل ۵ راسته است.
ـ راسته گل سرخ (Rosales)
ـ راسته چتریان (Umbellales)
ـ راسته مورد (Myrtales)
ـ راسته گل ساعتی (Passiflorales)
ـ راسته کاکتوسها (Cactales)
دو لپه ایهای پیوسته گلبرگ Sympetalae
این گیاهان بالغ بر ۵۰ هزار گونه هستند. گلبرگها در این گیاهان بهم پیوسته هستند. در اغلب پیوسته گلبرگها پرچمها به قسمت داخلی جام گل پیوستهاند. این گروه از گیاهان شامل ۱۱ راسته هستند که در سه گروه قرار می گیرند.
پیوسته گلبرگهای ۵ پیرامونی ، با تخمدان فوقانی و ۵ برچه.
ـ راسته اریکال (Ericales):
ابتدایی ترین راسته هستند، جام گل گاهی ناپیوسته ، نافه ۱۰ پرچمی و پرچمها غیر متصل به گلبرگها.
ـ راسته پامچال (Primulales):
جام گل پیوسته ، پرچمها به قسمت داخلی جام گل پیوسته اند.
ـ راسته خرمالو (Ebenales)
ـ راسته (Plumbaginales)
پیوسته گلبرگهای ۴ پیرامونی ، با تخمدان فوقانی و ۲ برچه.
ـ راسته Gentianales:
که از این راسته می توان به زیتون ، زبان گنجشک و یاسمن اشاره کرد.
ـ راسته Polemoniales:
که از این راسته می توان به گاو زبان ، سیب زمینی و گوجه فرنگی اشاره کرد.
ـ راسته Personales: که از این راسته می توان به گل میمون ، گل جالیز و کنجد اشاره کرد.
ـ راسته Lamiales:
که از این راسته می توان به نعنا، بارهنگ و شاه پسند اشاره کرد.
پیوسته گلبرگهای ۴ پیرامونی ، با تخمدان تحتانی و ۲ برچه.
ـ راسته گل استکانی (Campanulales):
که شامل گل استکانی و کدو است.
ـ راسته روناس (Rubiales):
که شامل تیره روناس و بداغ است.
ـ راسته گل مینا (Asterales):
که شامل تیره گل مینا ، تیره سنبل الطیب و تیره خواجه باشی می باشد.
دو لپه ایهای بی گلبرگ Monochlamideae
ـ راسته کازوآرینال (Casuarinales):
گیاهانی هستند درختی با ظاهری شبیه دم اسبیان و گلها یک جنسه می باشد.
ـ راسته آمنتال (Amentales):
در این راسته تیره های بید ، راش ، فندق و گردو قرار دارد.
ـ راسته گزنه (Urticales):
در این راسته تیره های گزنه ، توت ، نارون و شاهدانه قرار دارد.
ـ راسته دانه مرکزیان (Centrospermales):
در این راسته تیره های اسفناج ، گل میخک ، چغندر و لاله عباسی قرار دارد.
ـ راسته علف هفت بند (Polygonales):
در این راسته تیره های ترشک ، علف هفت بند و ریواس قرار دارد.
ـ راسته Santalales:
که در این راسته تیره معروف دارواش قرار دارد.
در اینجا جزوه پاورپوینت درس آزمایشگاه سیستماتیک گیاهی 2، بخش هفتم، در 43 صفحه برای شما عزیزان قرار داده شده است.
لینک دانلود مستقیم فایل در 43 صفحه
حجم فایل: 6.83 مگابایت

